La mejor música
sábado, 17 de diciembre de 2016
sábado, 10 de diciembre de 2016
Química del carbono
4Buckminsterfulerenos
1) Explica los motivos por los que el carbono es el elemento que forma mayor número de compuestos.
El carbono tiene las siguientes características que lo hacen diferente a otros elementos:
Tetravalencia: Tiene de poder unirse a 4 sustituyentes diferentes.
Concatenación: Es la capacidad del átomo de carbono de formar largas cadenas de Carbonos, enlazados entre si, lo que lo hace formar una gran cantidad de compuestos diferentes y presentar todos los tipos de isomería (isómeros: compuestos diferentes, pero con igual fórmula).
Fuentes: http://clickmica.fundaciondescubre.es/conoce/100-preguntas-100-respuestas/5-materiales/83-ipor-que-el-carbono-da-tantos-compuestos-distintos, https://es.answers.yahoo.com/question/index?qid=20120315045325AA86IAh, http://quimica.cubaeduca.cu/medias/interactividades/comptodcarbono/co/modulo_raiz_carbono_5.html.
2) Analiza las distintas formas alotrópicas del carbono, relacionando la estructura con las propiedades.
1. Diamante: su dureza y alta dispersión de la luz lo hacen útil para aplicaciones industriales y joyería
2. Grafito: es uno de los alótropos más comunes del carbono. Es un conductor eléctrico y se puede usar como material en los electrodos.
3. Carbono amorfo: nombre del carbono que no tiene una estructura cristalina. El carbono amorfo natural (como el hollín) contiene cristales microscópicos de grafito, algunas veces diamante.
4. Buckminsterfulerenos: descubiertos en un laboratorio en 1985. Recibieron el nombre por la similitud de su estructura alotrópica con las estructuras diseñadas por el científico Richard Buckminster.
5. Carbono vítreo: es un tipo de carbono no grafitizante, usado como material para electrodos en electroquímica, en crisoles de alta temperatura y como componente de dispositivos prostéticos.
6. Nanoespuma de carbono: Cada cúmulo es 6 nm de ancho, y tiene 4000 átomos de carbono, unidos en hojas similares a las del grafito. Es un mal conductor eléctrico.
7. Lonsdaleíta (diamante hexagonal): es un alótropo hexagonal del alótropo de carbono diamante, se forma a partir del grafito de los meteoritos al impactar con la Tierra. Ha sido sintetizado en el laboratorio, mediante compresión y calentamiento del grafito.
Productos especiales: como lubricantes, asfaltos, grasas para vehículos y productos de uso industrial.
Fuentes: https://mundoquimica.wordpress.com/164-2/, http://es.slideshare.net/anaacriado/aplicaciones-de-los-hidrocarburos.
7. Lonsdaleíta (diamante hexagonal): es un alótropo hexagonal del alótropo de carbono diamante, se forma a partir del grafito de los meteoritos al impactar con la Tierra. Ha sido sintetizado en el laboratorio, mediante compresión y calentamiento del grafito.
8. Carbono acetilénico lineal (LAC): El carbono acetilénico lineal (LAC) es un alótropo del carbono que tiene la estructura química -(C≡C)n- como una cadena repetitiva.
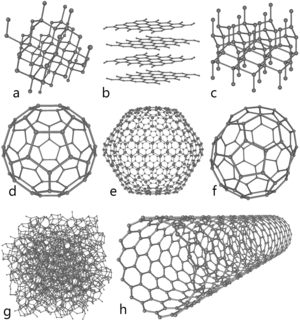
a) Diamante.
b) Grafito.
c) Lonsdaleíta,
d) C60 (Buckminsterfulereno o buckybola).
e) C540.
f) C70.
g) Carbono amorfo.
h) Nanotubo de carbono de pared simple o buckytubo.
Fuentes: https://es.wikipedia.org/wiki/Grafito, https://es.wikipedia.org/wiki/Al%C3%B3tropos_del_carbono#Variabilidad_del_carbono, http://quimica.laguia2000.com/quimica-inorganica/formas-alotropicas-del-carbono.
3) Describe las aplicaciones de hidrocarburos sencillos de especial interés.
Solo los de especial interés (si quiere que ponga más dígamelo, y si no, no hace falta que me diga nada):
Energéticos: que son combustibles específicos para transporte, la industria, la agricultura, la generación de corriente eléctrica y uso doméstico.

a) Diamante.
b) Grafito.
c) Lonsdaleíta,
d) C60 (Buckminsterfulereno o buckybola).
e) C540.
f) C70.
g) Carbono amorfo.
h) Nanotubo de carbono de pared simple o buckytubo.
Fuentes: https://es.wikipedia.org/wiki/Grafito, https://es.wikipedia.org/wiki/Al%C3%B3tropos_del_carbono#Variabilidad_del_carbono, http://quimica.laguia2000.com/quimica-inorganica/formas-alotropicas-del-carbono.
3) Describe las aplicaciones de hidrocarburos sencillos de especial interés.
Solo los de especial interés (si quiere que ponga más dígamelo, y si no, no hace falta que me diga nada):
Energéticos: que son combustibles específicos para transporte, la industria, la agricultura, la generación de corriente eléctrica y uso doméstico.
Productos especiales: como lubricantes, asfaltos, grasas para vehículos y productos de uso industrial.
Fuentes: https://mundoquimica.wordpress.com/164-2/, http://es.slideshare.net/anaacriado/aplicaciones-de-los-hidrocarburos.
Suscribirse a:
Entradas (Atom)